
Buat mengetahui Metode atom-atom dapat berikatan, Anda harus mempelajari susunan elektron di dalam suatu atom atau yang disebut konfigurasi elektron. Sebagaimana dijelaskan pada model atom Bohr, elektron bergerak mengelilingi inti atom menurut tingkat-tingkat Kekuatan tertentu yang disebut sebagai kulit-kulit atom.
Tingkat Kekuatan dalam suatu atom berturut-turut dilambangkan dengan K Buat kulit atom pertama (n=1), L Buat kulit atom kedua (n=2), M Buat kulit atom ke tiga (n=3), dan seterusnya. Berikut uraian tentang konfigurasi elektron yang dikutip dari Naskah Ilmu Pengetahuan Alam/Kementerian Pendidikan dan Kebudayaan Buat SMP/MTs Kelas IX Semester 2 yang ditulis Siti Zubaidah dkk.
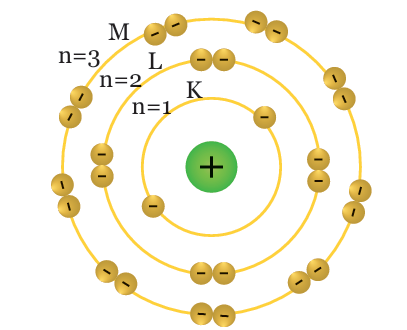
Keterangan gambar: Kulit-kulit atom dan jumlah elektron maksimal yang dapat menempati kulit tersebut.
Agar Anda lebih mudah mempelajari susunan elektron dalam suatu atom, kita gunakan istilah kulit-kulit atom sebagaimana teori Bohr Buat tingkat-tingkat Kekuatan. Dengan demikian suatu atom akan punya kulit K, kulit L, kulit M, dan seterusnya.
Tiap-tiap kulit atom ditempati oleh sejumlah elektron. Setiap kulit punya jumlah maksimum elektron yang dapat menempatinya.
Misalnya kulit K, maksimum hanya dapat ditempati oleh 2 elektron. Apabila atom tersebut punya elektron lebih dari 2, elektron berikutnya akan menempati kulit yang berikutnya. Posisi elektron pada kulit-kulit atom dimulai dari kulit terdalam atau yang mempunyai Kekuatan paling rendah.
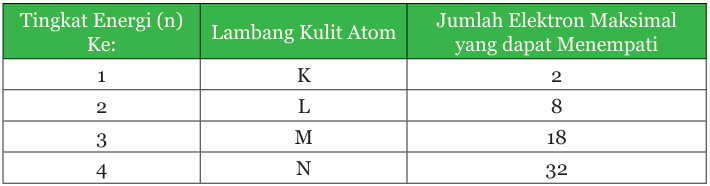
Keterangan tabel: Kulit atom dan jumlah elektron yang dapat menempati kulit tersebut.
Berdasarkan tabel di atas, perhatikan jumlah elektron pada tiap-tiap kulit beberapa atom berikut.
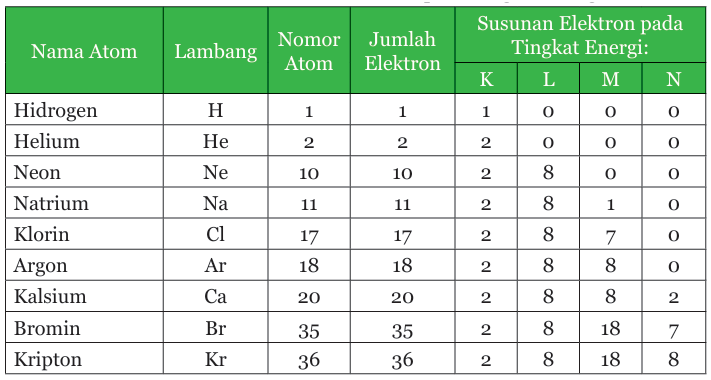
Keterangan tabel: Susunan elektron atom pada tingkat Kekuatan.
Posisi elektron secara berurutan dimulai dari kulit K, kemudian ke kulit atom yang lebih tinggi. Pada Misalnya di atas, atom helium (He), natrium (Na), dan klor (Cl), punya konfigurasi electron sesuai dengan urutan jumlah elektron yang dapat menempati kulit K, L, dan M.
Pada atom Ca yang punya 20 elektron, kulit atom K dan L berturut-turut ditempati oleh 2 dan 8 elektron sehingga tersisa 10 elektron. Walaupun kulit M dapat ditempati 18 elektron, tetapi jumlah elektron yang tersisa hanya 10.
Karena itu, sebanyak 8 elektron akan menempati kulit M terlebih dahulu dan 2 elektron akan menempati kulit N. Hal ini disebabkan penempatan 8 elektron pada kulit M dan 2 elektron pada kulit N lebih Kukuh dibandingkan penempatan 10 elektron sekaligus pada kulit M.
Apabila jumlah elektron yang tersisa setelah K dan L lebih dari 18 electron, kulit atom M akan ditempati 18 elektron. Perhatikan Misalnya konfigurasi atom bromin dan kripton. Intinya, elektron akan berada pada setiap kulit hingga membentuk susunan yang paling Kukuh. (Z-2)
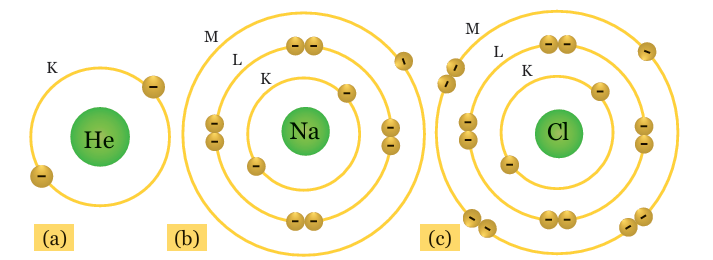
Keterangan gambar: Konfigurasi elektron pada atom H, atom Na, dan atom Cl.
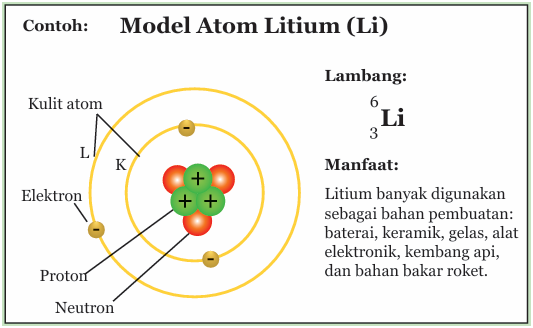
Keterangan gambar: Model atom Litium (Li).




